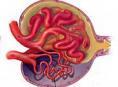
介绍
局灶性节段性肾小球硬化(FSGS)是儿童和成人肾病综合征(NS)常见的原发性肾小球疾病,其组织病理学特征是肾小球节段性瘢痕,伴或不伴肾小球毛细血管内泡沫细胞形成和粘连。局灶性是指只有部分肾小球被累及(受累肾小球
最新文章
症状
本病多发生在儿童及青少年,男性稍多于女性。少数患者发病前有上呼吸道感染或过敏反应。临床首发症状最多见的是肾病综合征,约2/3的患者有大量蛋白尿和严重水肿,尿蛋白量可在1~30克/天,约50%以上的患者有血尿,镜下血尿多见,偶见肉眼血尿。成人中30%~50%患者有轻度持续性高血压或表现为慢性肾炎综合征,患者24小时尿蛋白
病因
FSGS有多方面的致病因素。如中毒损伤、体液免疫及血流动力学改变等,均可导致毛细血管壁损伤,使大分子蛋白产生并滞留,免疫球蛋白沉积后再与C1q和C3结合,引起足突细胞退变并与基膜相脱离。
残余肾单位血流动力学发生改变,引起肾小球毛细血管代偿性高血压、高灌注及高滤过,造成上皮细胞及内皮细胞损伤,系膜细胞功能异常,从而导致进行性局灶性节段性硬化。这种病理过程可因摄入大量蛋白而加重,限制蛋白摄入和降血压治疗而减轻。内皮细胞损伤引起血小板聚集及微血栓形成,而加重病变的发展;许多FSGS的发生与这种发病机制有关,如慢性链球菌感染后肾炎、慢性移植肾排异、反流性肾病及镇痛药肾病等。
检查
1.尿常规检查
镜下血尿、蛋白尿;常有无菌性白细胞尿、葡萄糖尿;肾小管功能受损者有氨基酸尿及磷酸盐尿,其发生率高于其他类型的NS。
2.血液检查
有明显低白蛋白血症,血浆白蛋白通常低于25g/L,少数可达10g/L以下;肾小球滤过率(GFR)下降、血尿素氮、肌酐升高;多数患者有高脂血症,血清C3通常正常,IgG水平降低,C1q大多正常,10%~30%患者有循环免疫复合物阳性;血容量减少时,可造成血细胞比容上升,白细胞及分类正常,血小板轻度增高;水潴留会造成血钠浓度降低,长期限钠或获得性肾上腺功能不全,也会导致血钠浓度降低;高脂血症会造成假性低钠血症,由于血小板能在体外释放钾离子。所以,血小板增多时也会造成假性高钾血症。
3.肾活检光镜检查
典型的FSGS病变特征为肾小球局灶性节段性损害,病变累及少数肾小球及肾小球部分节段的玻璃样硬化,病变常从皮质深层或近髓部位肾小球开始,逐渐扩展至肾皮质,病变肾小球呈节段性硬化,未受累的肾小球正常或系膜基质增加,透明样物质沉积于受损毛细血管襻的内皮细胞下,硬化区偶有泡沫细胞形成,常见局限性上皮细胞增生。
4.电镜检查
有大量蛋白尿的病例,大部分或全部肾小球显示弥漫性或节段性足突改变,早期在毛细血管壁和(或)系膜区可见泡沫细胞,系膜基质增加及部分毛细血管塌陷,内皮细胞下及系膜区有电子致密物沉积,系膜细胞增生,大块的电子致密物与光镜下的玻璃样变及免疫荧光IgM和C3沉积相对应,球旁系膜区及内皮细胞下亦可见细颗粒状电子致密物沉积。
5.免疫荧光检查
在硬化或坏死区可发现C3或IgM及C1q呈不规则、颗粒状或结节状分布。无病变的肾小球呈阴性,偶尔系膜区有IgM及C3分布,IgG、IgA少见。
鉴别
1.非塌陷性局灶节段性肾小球硬化目前对于CG及FSGS的关系仍有争议。有的学者认为CG是独立的疾病,大部分学者认为CG是非塌陷性局灶节段性肾小球硬化(NC-FSGS)的严重类型。它们间的区别在于临床上CG患者中尿蛋白大于10g/d的人数比NC-FSGS明显多;发病时肾功能不全比例高,肾功能恶化快。其病理区别是:①CG为肾小球毛细血管塌陷,基质物明显扩张,病变节段很少与肾小球囊粘连,而NC-FSGS相反。②CG上皮细胞肥大明显并有上皮细胞内颗粒。③CG的病变节段很少位于小球血管极,而这种改变在NC-FSGS很常见。④CG的小管间质炎症、萎缩及纤维化较NC-FSGS明显。免疫学证实,CG的肾小球肾小管的增生标志多于NC-FSGS。尽管如此,由于CG的病变多呈节段局灶分布,目前仍将其归入特发性局灶节段性肾小球硬化,但作为特殊亚型,其临床表现及形态学改变与特发性FSGS有所不同。
2.人类免疫缺陷病毒相关性肾病(艾滋病)人类免疫缺陷病毒相关性肾病(HIV-AN)是AIDS患者肾脏合并症,多见于HIV感染的早期,其他严重感染之前。其肾脏临床表现、光镜、免疫荧光方面的病理特点与特发性塌陷性肾小球病表现相似,甚难区别。ICG与HIV-AN病理区别主要在于电镜表现。电镜下HIV-AN的肾小球内皮细胞、间质白细胞内有大量的管网状包涵物(TRI)。TRI主要在内质网扩张池、环核池及高尔基体池。80%~90%的HIV-AN患者肾小球内皮细胞内存在TRI,而CG患者仅有10%发现TRI。故依据患者有无HIV易感因素(如静脉毒品滥用、同性恋、HIV高发地区及高发人群),早期HIV检测及抗HIV抗体的检测,并结合HIV的其他临床表现(如无症状性感染、持续性淋巴结肿大、继发性肿瘤)可鉴别CG和HIV-AN。
3.局灶及节段性增生性肾小球肾炎其后期病变亦可类似本病之病理改变,此病变也多见于IgA肾病、局灶增生性狼疮性肾炎及紫癜性肾炎、小血管炎等。其病理改变为局灶性节段性内皮细胞及系膜细胞增生,伴局灶及节段分布的新月体形成。根据其相应的临床表现及特征性免疫荧光所见,可作鉴别。
4.局灶性肾小球纤维化与本病在病理上是不同的概念,较少见。病变肾小球皱缩呈胶原纤维染色,嗜银及PAS染色阴性。
5.微小病变肾病目前多数学者认为MCD与FSGS为两种不同类型的肾脏病变。FSGS早期,病变多局限于皮髓交界区,因而肾活检检查常因穿不到该部位而与MCD混淆。故应注意两者的鉴别,如糖皮质激素不敏感者及年龄较大者,可能是FSGS早期,必要时重复进行肾活检。连续切片可提高诊断率。MCD光镜下肾小球很少有形态学改变。肾小管上皮细胞内可见双折光的脂肪滴,近曲小管上皮细胞可见有空泡样改变。电镜下上皮细胞肿胀,足突融合成片状,滤孔闭塞,伴上皮细胞空泡变性、微绒毛形态、蛋白吸收滴及溶酶体增加。免疫荧光检查多为阴性,偶见IgG和(或)IgM、IgA、C3沉着。
此外,超过40岁的正常人群,被膜下皮质可有硬化荒废的肾小球,应注意与本病区别。
并发症
1.感染与蛋白质丢失、营养不良、免疫功能紊乱及应用糖皮质激素治疗有关。感染是肾病综合征的常见并发症,由于应用糖皮质激素,其感染的临床征象常不明显,尽管目前已有多种抗生素可供选择,但若治疗不及时或不彻底,感染仍是导致病情复发和疗效不佳的主要原因,甚至导致病人死亡,应予以高度重视。
2.血栓、栓塞并发症由于血液浓缩及高脂血症造成血液黏稠度增加;此外,因某些蛋白质丢失,及肝代偿性合成蛋白增加,引起机体凝血、抗凝和纤溶系统失衡。因此,易发生血栓、栓塞并发症。
3.急性肾衰竭肾病综合征病人可因有效血容量不足而致肾血流量下降,诱发肾前性氮质血症。又因肾间质高度水肿压迫肾小管以及大量蛋白管型阻塞肾小管和肾小管腔内高压,间接引起肾小球滤过率骤然减少,导致急性肾衰竭。
4.蛋白质及脂肪代谢紊乱长期低蛋白血症可导致营养不良、小儿生长发育迟缓;免疫球蛋白减少造成机体免疫力低下、易致感染;金属结合蛋白丢失可使微量元素(铁、铜、锌等)缺乏;内分泌素结合蛋白不足可诱发内分泌紊乱;药物结合蛋白减少可能影响某些药物的药动学(使血浆游离药物浓度增加、排泄加速),影响药物疗效。高脂血症中血液黏稠度增加,促进血栓、栓塞并发症的发生,还将增加心血管系统并发症,并可促进肾小球硬化和肾小管-间质病变的发生,促进肾脏病变的慢性进展。
治疗
1.糖皮质激素
应在出现激素抵抗前及时用泼尼松(强的松)治疗。一般获得完全缓解的平均时间为3~4个月。因此成人FSCS所导致的NS在经过6个月的泼尼松治疗仍未缓解者,才称之为激素抵抗。对于老年人,大部分学者主张隔天泼尼松治疗,持续3~5个月。对于激素依赖、抵抗和复发者,泼尼松加间断环磷酰胺冲击治疗可增加缓解率,环磷酰胺总量不宜超过12克。
2.环孢素(CsA)和可乐必复(FK506)
环孢素常用剂量治疗6个月后可减少尿蛋白并诱导缓解,但减量或停药时常复发。所以,维持缓解应长期应用。因该药有肾毒性,使用过程中应注意监测血肌酐,根据情况调整药量。可乐必复的作用机制与环孢素相似,可与激素合用。常用于环孢素治疗无效或依赖者。
3.细胞毒类药物(环磷酰胺和苯丁酸氧芥)
可作为二级疗法,但有待临床观察证实其疗效。
4.血浆置换及蛋白吸附疗法
可应用于复发性FSGS的肾移植患者。血浆置换或蛋白吸附可减少循环免疫因子,使尿蛋白暂时减轻。
5.NSAIDs(非甾体类抗炎药)及ACEI(血管紧张素转换酶抑制剂)
可通过降低GFR而减轻蛋白尿及高脂蛋白血症。
6.其他药物
其他如硫唑嘌呤、霉酚酸酯(MMF)、ACEI和ARB(血管紧张素Ⅱ受体阻滞剂)等药物也可选择使用。
预防
本病临床病程变化较大,病程转归各不相同,所以预防要从自身健康着手,平时避免劳累,合理饮食,科学锻炼,增强体质,提高机体免疫力,以防疾病发生。对于已患和出现并发症的病人,应对原发病及并发症进行积极有效的预防和治疗。如一旦发现感染,应及时选用对致病菌敏感、强效且无肾毒性的抗生素治疗,有明确感染灶者应尽快去除。当发现血浆白蛋白浓度低于20g/L时,提示高凝状态已存在,即应开始预防性抗凝治疗。对已发生血栓、栓塞者应尽早(6h内效果最佳,但3天内仍可望有效)给予尿激酶或链激酶全身或局部溶栓,同时配合抗凝治疗。并发急性肾衰竭如处理不当可危及生命,及时给予正确处理,大多数病人可望恢复。
相关疾病
高血压 高血脂 低钠血症 高钾血症 血管炎 狼疮性肾炎 肾功能衰竭 IgA肾病 尿路感染 紫癜性肾炎 肾小球肾炎 艾滋病 中毒 肾移植 免疫缺陷病 动脉硬化 高脂蛋白血症 梗阻性肾病 慢性肾炎 膜性肾病 肾病综合征 血尿 高脂血症 水肿 肿胀 血栓形成 子痫